ę╗Īó╩ņŠÜėøæøęÄ(gu©®)┬╔╩Ūæ¬(y©®ng)ė├Ą─Ū░╠ß
╦ßēA¹}▓┐Ęųļm╚╗Ņ}ą═▒ŖČÓ���Ż¼╚ńŻ║Ķbäe����Īó═ŲöÓ����Īó│²ļs……���Ż¼Ą½╩Ū▀@ą®æ¬(y©®ng)ė├ļx▓╗ķ_ūŅ╗∙ĄA(ch©│)Ą─ų¬ūR³cŻ║╝┤Ż║ī”╦ßēA¹}╗»īW(xu©”)ąį┘|(zh©¼)Ą─╩ņŠÜėøæøĪŻ
═©▀^īW(xu©”)┴Ģ(x©¬)┐╔ų¬Ż║╦ߥ─═©ąįėą╬Õ³c��ĪóēA║═¹}Ą─═©ąįĖ„ėą╦─³c�ĪŻī”ė┌▀@ą®╗»īW(xu©”)ąį┘|(zh©¼)▒žĒÜ╝ėęįÅŖ╗»ėøæø║═ņ`╗Ņėøæø���ĪŻ┐╔▓╔ė├łD▒ĒėøæøĘ©ęį╝░ūā╩ĮėøæøĘ©Ą╚���ĪŻ
╚ńŻ║īó╦ßēA¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)ØŌ┐s×ķŽ┬łDėøæø▌^║├(łD▒ĒėøæøĘ©)
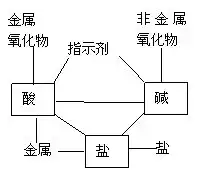
į┌┤╦╗∙ĄA(ch©│)╔Ž��Ż¼į┘ū÷ūā╩ĮŠÜ┴Ģ(x©¬)���Ż¼į÷╝ėī”╗»īW(xu©”)ąį┘|(zh©¼)Ą─ČÓĮŪČ╚ėøæø(ūā╩ĮėøæøĘ©)��ĪŻ╚ńŻ║
(1)╔·│╔¹}║═╦«Ą─ęÄ(gu©®)┬╔�Ż¼ę╗Č©╩Ūųą║═Ę┤æ¬(y©®ng)åß?
(2)į┌╦ßēA¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)ųą���Ż¼╔·│╔¹}Ą─ęÄ(gu©®)┬╔ėąÄūŚlĄ╚���ĪŻ
═©▀^╚ń╔ŽŠÜ┴Ģ(x©¬)�Ż¼╝┤┐╔ŲĄĮ╝ėÅŖų¬ūRĄ─═¼╗»║═«É╗»Ą─ū„ė├���ĪŻ
Č■ĪóšŲ╬š“ęÄ(gu©®)Šž”�����Ż¼┐╔│╔“ĘĮłA”
ėøæøūĪęį╔ŽęÄ(gu©®)┬╔Š═┐╔ęį╩ņŠÜæ¬(y©®ng)ė├┴╦åß?«ö(d©Īng)╚╗▓╗─▄ĪŻį┌┤¾┴┐ŠÜ┴Ģ(x©¬)ųą═¼īW(xu©”)éā░l(f©Ī)¼F(xi©żn)ęį╔ŽęÄ(gu©®)┬╔ųąėą║▄ČÓ╩Ūėą “ęÄ(gu©®)Šž” ėąŚl╝■Ą─����ĪŻę“┤╦į┌ėøūĪęÄ(gu©®)┬╔Ą─Ū░╠ߎ┬��Ż¼▀Ćę¬ėøūĪęÄ(gu©®)┬╔æ¬(y©®ng)ė├Ą─Śl╝■���Ż¼▀@śė▓┼─▄ū÷ĄĮėąĄ─Ę┼╩ĖĄ─æ¬(y©®ng)ė├ĪŻ▒╚╚ńŻ║┐╔Ė∙ō■(j©┤)▓╗═¼Ę┤æ¬(y©®ng)ŅÉą═üĒņ`╗ŅėøæøėąĻP(gu©Īn)Ę┤æ¬(y©®ng)Ą─Śl╝■����ĪŻÜw╝{╚ńŽ┬Ż║
└²╚ńŻ║īæ│÷Ž┬┴ą╬’┘|(zh©¼)ųąā╔ā╔ų«ķg─▄░l(f©Ī)╔·Ę┤æ¬(y©®ng)Ą─╗»īW(xu©”)ĘĮ│╠╩Į����ĪŻ
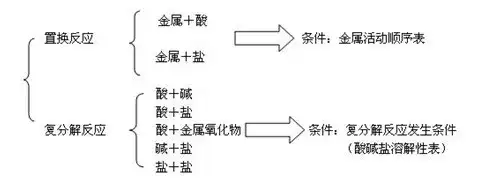
ĶFĪóč§╗»ĶF�����Īó¤²ēA╚▄ę║����ĪóŽĪ┴“╦ß����Īó┴“╦ßŃ~╚▄ę║Īó┬╚╗»õ^╚▄ę║�ĪóČ■č§╗»╠╝
╦╝┬Ę³cō▄Ż║
ĮŌ╬÷Ż║A�Īó═©▀^╬’┘|(zh©¼)ĘųŅÉŻ¼’@╚╗ę└┤╬Ę¹║ŽēAąį�Īóųąąį����Īó╦ßąįŻ¼«ö(d©Īng)╚╗╝ė╩»╚’įćę║Ķbäe�����ĪŻ
BĪó ═©▀^ė^▓ņ░l(f©Ī)¼F(xi©żn)Ż║Na2CO3ė÷╦ß(H+)«a(ch©Żn)╔·ÜŌ¾w����Ż¼Č°AgNO3ė÷CL-«a(ch©Żn)╔·│┴ĄĒ��Ż¼Č°KNO3ė÷¹}╦ߤo¼F(xi©żn)Ž¾���Ż¼╣╩╝ė¹}╦ßüĒĶbäe���ĪŻ
CĪóė╔╔Ž┐╔ų¬Ż║K2CO3ė÷╦ß(H+)«a(ch©Żn)╔·ÜŌ¾w�Ż¼BaCl2╚▄ę║ė÷SO42-ėą│┴ĄĒ��Ż¼Č°NaCl╚▄ę║ė÷ŽĪ┴“╦ߤo¼F(xi©żn)Ž¾�����Ż¼╣╩╝ėŽĪ┴“╦ßüĒĶbäeĪŻ
D�����ĪóCa(OH)2╚▄ę║ė÷CO32-ėą│┴ĄĒ�����Ż¼ŽĪHCl ė÷CO32-ėąÜŌ¾w�����Ż¼Č°NaOH ė÷CO32-¤o├„’@¼F(xi©żn)Ž¾��Ż¼╣╩╝ėNa2CO3╗“K2CO3Ķbäe�ĪŻ
E�����Īóė^▓ņ┐╔ų¬Ż║NH4+ė÷OH-«a(ch©Żn)╔·░▒ÜŌ����Ż¼Č°Ba2+ė÷CO32-���ĪóSO42-Š∙ėą│┴ĄĒ«a(ch©Żn)╔·��Ż¼╚Īśė║¾ĘųäeĄ╬╝ėBa(OH)2╚▄ę║��Ż¼ų╗ėąÜŌ¾w«a(ch©Żn)╔·Ą─╩ŪNH4NO3��Ż¼═¼ĢrėąÜŌ¾w║═│┴ĄĒ«a(ch©Żn)╔·Ą─╩Ū(NH4)2SO4Ż¼ų╗ėą│┴ĄĒ«a(ch©Żn)╔·Ą─╩ŪNa2CO3����Ż¼¤o¼F(xi©żn)Ž¾Ą─╩ŪNaCl����ĪŻ
į┌īŹļHæ¬(y©®ng)ė├ųą�Ż¼═¼īW(xu©”)éā▀Ć┐╔ęįīóĶbäeŅ}░┤ę╗┤╬ąįĶbäeĪóČÓ┤╬ąįĶbäe��Īó▓╗╝ėŲõ╦¹įćä®Ķbäe�Īóā╔ā╔╗ņ║ŽĶbäeĄ╚▀MąąĘųŅÉŻ¼Ė∙ō■(j©┤)Ė„ūį¬ÜėąĄ─╠ž³c���Ż¼┐éĮY(ji©”)ĮŌŅ}╝╝Ū╔Ż¼Å─Č°▀_ĄĮ╚½├µšŲ╬š▓╗═¼ĶbäeŅÉą═Ą──┐Ą─��ĪŻ
└²Č■Ż║▀xė├║Ž▀mĄ─ĘĮĘ©│²╚źŽ┬┴ą╬’┘|(zh©¼)ųąĄ─╔┘┴┐ļs┘|(zh©¼)
(1)│²╚ź╔·╩»╗ęųąĄ─╠╝╦ßŌ}
(2)│²╚ź┬╚╗»ŌøŠ¦¾wųąĄ─╠╝╦ßŌø
(3)│²╚ź╠╝╦ßŌ}╣╠¾wųąĄ─╠╝╦ßŌc
(4)│²╚źę╗č§╗»╠╝ųąĄ─Č■č§╗»╠╝
(5)│²╚ź┬╚╗»Ōc╚▄ę║ųąĄ─┴“╦ßŃ~
(6)│²╚źCuĘ█ųąĄ─FeĘ█
╦╝┬Ę³cō▄Ż║
│²ļsĄ─įŁät╩ŪŻ║▓╗į÷(▓╗į÷╝ėą┬ļs┘|(zh©¼))����Īó▓╗£p(▓╗£p╔┘įŁ╬’┘|(zh©¼)Ą─┴┐)Īó▓╗ūā(▓╗Ė─ūāįŁ╬’┘|(zh©¼)ĀŅæB(t©żi))�ĪóęūĘų(│²ļs║¾ęūė┌Ęųļx)ĪóŽ╚╬’║¾╗»(╬’└ĒĘĮĘ©ā×(y©Łu)Ž╚���Ż¼Ųõ┤╬╗»īW(xu©”)ĘĮĘ©)����ĪŻæ¬(y©®ng)ė├ųąėą▐D(zhu©Żn)╗»Ę©Īó│┴ĄĒĘ©���Īó╬³╩šĘ©Īó▀^×VĘ©���Īó╚▄ĮŌĘ©Ą╚ČÓĘN│²ļsĘĮĘ©ĪŻ
ĮŌ╬÷Ż║(1)═©▀^Ė▀£ž╝ė¤ß╗“ūŲ¤²Ą─ĘĮĘ©��Ż¼╝╚─▄│²╚ź╠╝╦ßŌ}�Ż¼ėų─▄Ą├ĄĮĖ³ČÓ╔·╩»╗ęĪŻ
(2)┐╔╝ė╚ļ▀m┴┐ŽĪ¹}╦ß│õĘųĘ┤æ¬(y©®ng)║¾����Ż¼į┘š¶░l(f©Ī)ĪŻ
(3)┐╔▓╔ė├Ž╚╝ė▀m┴┐╦«╚▄ĮŌ���Ż¼į┘▀^×VĄ─ĘĮĘ©���ĪŻ
(4)┐╔▓╔ė├═©▀^¤ļ¤ßĄ─╠╝īė╗“═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©����ĪŻĄ½’@╚╗═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©Š▀ėą╬³╩šļs┘|(zh©¼)ÅžĄū��Īó▓┘ū„║åå╬┐ņĮ▌Ą╚ā×(y©Łu)³c��ĪŻ
(5)ė╔ė┌║¼ėąCu2+��ĪóSO42-ā╔ĘNļs┘|(zh©¼)ļxūė��Ż¼╣╩┐╔▓╔ė├═¼Ģr│┴ĄĒĘ©ĪŻ╝ė╚ļ▀m┴┐Üõč§╗»õ^╚▄ę║║¾����Ż¼▀^×V╝┤┐╔Ą├┬╚╗»Ōc╚▄ę║ĪŻ
(6)ė╔ė┌Fe�ĪóCuĘųäe┼┼į┌Įī┘╗ŅäėĒśą“▒ĒųąHĄ─Ū░║¾Ż¼╦∙ęį┐╔▓╔ė├╝ė╚ļūŃ┴┐ŽĪ¹}╦ß╗“ŽĪ┴“╦ß╚▄ĮŌ▓ó▀^×VĄ─ĘĮĘ©üĒīŹ¼F(xi©żn)��ĪŻę▓┐╔▓╔ė├╝ėūŃ┴┐┴“╦ßŃ~╚▄ę║▓ó▀^×VĄ─ĘĮĘ©���ĪŻ
└²╚²���Īóėąę╗╣╠¾w╗ņ║Ž╬’����Ż¼┐╔─▄║¼ėąK2CO3����ĪóK2SO4ĪóCuSO4���ĪóCaCl2�����ĪóKNO3Ą╚╬’┘|(zh©¼)ųąĄ─ę╗ĘN╗“ÄūĘN���Ż¼īó╗ņ║Ž╬’╚▄ė┌╦«Ż¼Ą├¤o╔½╚▄ę║�Ż¼«ö(d©Īng)?sh©┤)╬╚ļŽ§╦ßõ^╚▄ę║ĢrŻ¼ėą░ū╔½│┴ĄĒ«a(ch©Żn)╔·���Ż¼į┘╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌ�Ż¼ätįō╗ņ║Ž╬’ųąę╗Č©║¼ėą____________ę╗Č©▓╗║¼ėą_______________┐╔─▄║¼ėą_____________.
╦╝┬Ę³cō▄Ż║
═ŲöÓŅ}╦∙ė├ĄĮĄ─ų¬ūRā”éõėą╚ńŽ┬Äū³cŻ║(1)╬’┘|(zh©¼)Ą─╠ž╩Ō╔½æB(t©żi)�����Īó╚▄ĮŌąį(░³└©╬’┘|(zh©¼)į┌╦«╗“╦ßųąĄ─╚▄ĮŌąį)ĪŻ╚ńŻ║Ń~ļxūė╚▄ę║×ķ╦{╔½�����Ż¼ĶFļxūė╚▄ę║×ķ³S╔½Ą╚��Ż¼│ŻęŖ░ū╔½│┴ĄĒėą╠╝╦ßŌ}�����Īó╠╝╦ßõ^Īó╠╝╦ßŃy�Īó┬╚╗»Ńy��Īó┴“╦ßõ^�����ĪóÜõč§╗»µVĄ╚����ĪŻ╦{╔½│┴ĄĒėąÜõč§╗»Ń~��Ż¼╝t║ų╔½│┴ĄĒėąÜõč§╗»ĶF�ĪŻ│§ųą▓╗╚▄ė┌╦ߥ─│┴ĄĒėą┬╚╗»Ńy��Īó┴“╦ßõ^�����ĪŻ(2)Ģ■┼ąöÓ╬’┘|(zh©¼)ų«ķg─▄ʱ░l(f©Ī)╔·Ę┤æ¬(y©®ng)���ĪŻ(3)╚²ĘNļxūė(┴“╦ßĖ∙���Īó╠╝╦ßĖ∙Īó┬╚ļxūė)ĶbČ©Ą─š²─µ═Ų└Ē���ĪŻ(4)ī”ė┌ųž³cį~šZĄ─└ĒĮŌ─▄┴”ĪŻ╚ńŻ║“╚½▓┐╚▄”���Īó“▓┐Ęų╚▄”Īó“╚½▓╗╚▄”Ą╚į~Ą─└ĒĮŌ����ĪŻę╗Ą└║├Ą─═ŲöÓŅ}š²╩Ūī”ė┌ęį╔Žų¬ūR³cšŲ╬š│╠Č╚Ą─ŠC║Žąį┐╝▓ņĪŻ
ĮŌ╬÷Ż║═ŲöÓŅ}Ą─ĮŌ┤ę└ō■(j©┤)╩Ū╬’┘|(zh©¼)Ą─╠žš„Ę┤æ¬(y©®ng)║═Ąõą═Ą─īŹ“×¼F(xi©żn)Ž¾����ĪŻ┤╦Ņ}ė╔╚▄ė┌╦«Ą├ĄĮ“¤o╔½╚▄ę║”┐╔ų¬Ż║CuSO4(╦{╔½╚▄ę║)ę╗Č©▓╗┤µį┌;═¼ĢrK2CO3����ĪóCaCl2ė╔ė┌ŽÓė÷Ģ■«a(ch©Żn)╔·│┴ĄĒŻ¼╦∙ęįK2CO3�ĪóCaCl2╗“┤µŲõę╗╗“Š∙▓╗┤µį┌���ĪŻė╔“Ą╬╝ėŽ§╦ßõ^╚▄ę║Ģr��Ż¼ėą░ū╔½│┴ĄĒ«a(ch©Żn)╔·”┐╔ų¬Ż║│┴ĄĒėą┐╔─▄üĒūįŽ§╦ßõ^┼cK2CO3╗“K2SO4Ę┤æ¬(y©®ng)╔·│╔Ą─╠╝╦ßõ^Īó┴“╦ßõ^│┴ĄĒųąĄ─ę╗š▀╗“ā╔š▀�ĪŻė╔“╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌ”┐╔ų¬Ż║╠╝╦ßõ^����Īó┴“╦ßõ^Š∙┤µį┌���Ż¼▀MČ°═Ų│÷K2CO3����ĪóK2SO4Š∙┤µį┌�ĪŻę“×ķK2CO3┤µį┌���Ż¼╦∙ęįCaCl2ę╗Č©▓╗┤µį┌�����ĪŻČ°KNO3ė╔ė┌┤µį┌┼cʱ���Ż¼Š∙▓╗Ģ■ī”ęį╔ŽĶbäe═ŲöÓįņ│╔ė░Ēæ����Ż¼╦∙ęįKNO3┐╔─▄┤µį┌Ż¼ę▓┐╔ęįšf┐╔─▄▓╗┤µį┌�����ĪŻ
┤╦Ņ}�����Ż¼į┌ŠÜ┴Ģ(x©¬)▀^│╠ųą�����Ż¼═Ļ╚½┐╔ęį┬į╝ėĖ─äė�ĪŻ╚ńŻ║╚¶“│┴ĄĒ╚½▓┐╚▄ĮŌ”═ŲöÓĮY(ji©”)╣¹į§śė?╚¶“│┴ĄĒ╚½▓╗╚▄”═ŲöÓĮY(ji©”)╣¹ėųĢ■į§śė?……ĪŻ═¼īW(xu©”)éāę╗Ą®šŲ╬š┴╦▀@ĘNę╗Ņ}ČÓūā����Īóę╗Ņ}ČÓū÷Ą─īW(xu©”)┴Ģ(x©¬)ĘĮĘ©��Ż¼ī”ė┌╠ßĖ▀Å═(f©┤)┴Ģ(x©¬)ą¦╣¹▒ž╚╗┐╔ęįŲĄĮęį³cĦ├µĄ─▌Ś╔õū„ė├����ĪŻ
┐éų«Ż¼╦ßēA¹}▓┐ĘųĄ─ųž³c║═ļy³c╩Ūš¹éĆ│§ųą╗»īW(xu©”)ųą║─┘MĢrķg║═Š½┴”ūŅČÓĄ─����Ż¼ų╗ėąūŃē“Ą─ųžęĢ║═▀Mąą▒žę¬Ą─īW(xu©”)┴Ģ(x©¬)▓┼─▄į┌╝┤īóĄĮüĒĄ─┐╝įćųąū÷ĄĮ│╔┐āĘĆ(w©¦n)ųąėą╔²ĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįO(sh©©)éõįLå¢ųą┐╝ŠW(w©Żng)����Ż¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤











